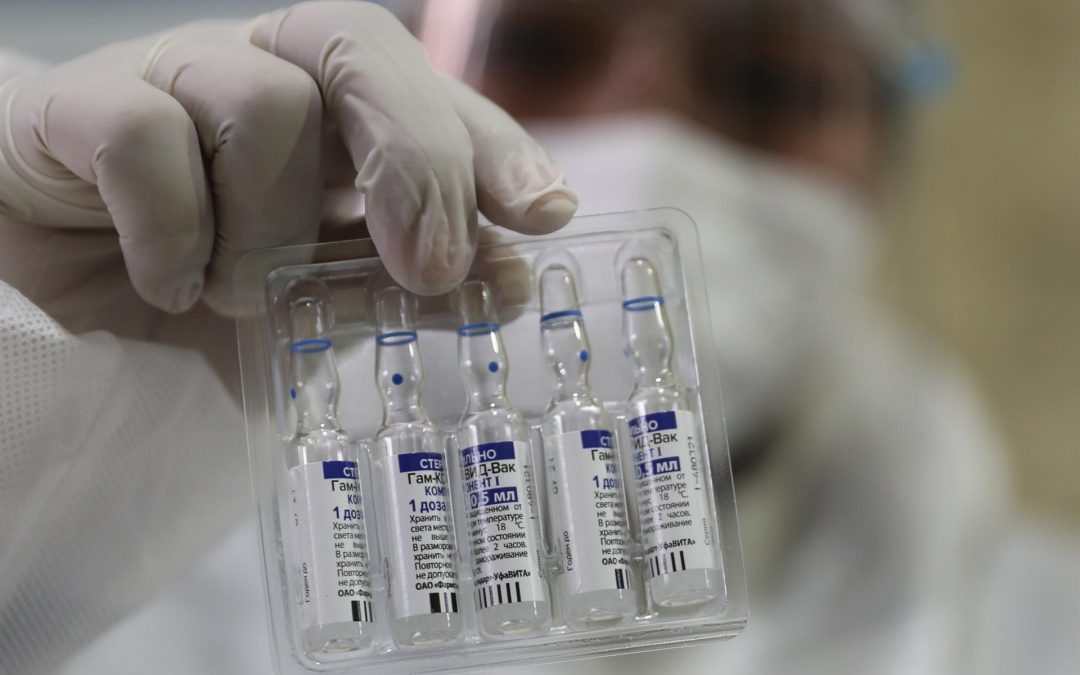
През нощта срещу четвъртък страните от ЕС и Европейският парламент постигнаха споразумение, което трябва да прочисти повече от 20-годишното законодателство на ЕС за лекарствата.
По този начин Дания реши една от най-деликатните задачи по време на датското председателство на ЕС, което продължава до 1 януари.
Тук Дания, със силна фармацевтична индустрия, водена от Novo Nordisk, имаше други интереси от редица страни от ЕС в Южна и Източна Европа, които основно желаеха по-евтини лекарства за гражданите.
Министърът на вътрешните работи и здравеопазването Sophie Løhde (V) смята, че е успяло да се постигне споразумение, което ще бъде „в полза на милиони европейци и ще укрепи способността на Европа да развива лекарствата на бъдещето“.
– С днешното споразумение поставяме нова посока за европейската здравна политика, при която осигуряваме по-бърз достъп до лечение, по-малко бюрокрация и по-силни рамки за конкурентоспособна life science индустрия в Европа, казва Sophie Løhde в писмен коментар.
Dansk Industri (DI) смята, че споразумението е по-добро от очакваното, но все пак е стъпка в грешната посока, погледнато от гледна точка на индустрията.
Централният въпрос в преговорите беше колко дълга да бъде общата защита на данните и пазара за нови лекарства.
В САЩ периодът е 12 години.
Това означава, че фармацевтичните компании имат 12 години, през които могат да печелят пари от новоразработени продукти без конкуренция от копия.
Това е добре за компаниите, но може да бъде скъпо за потребителите.
Затова редица страни от ЕС без големи фармацевтични компании пожелаха да съкратят периода, за да получат по-бърз достъп до евтини лекарства.
Периодът на защита в ЕС днес е общо десет години, когато фармацевтична компания пусне на пазара ново лекарство.
Тоест с две години по-кратък, отколкото в САЩ.
Европейската комисия предложи през 2023 г. да съкрати периода с две години в своето предложение за споразумението, което сега е постигнато.
Но с възможност периодът отново да бъде удължен с две години, ако новото лекарство бъде пуснато на пазара във всички държави членки на ЕС.
До там обаче новото споразумение не стига.
Страните от ЕС и Европейският парламент се спряха на намаляване на общия период на защита на данните и пазара от десет на девет години.
Но с възможност за още една година допълнителна пазарна защита за „иновативни“ лекарства, които отговарят на редица критерии.
Главният изпълнителен директор на DI Lars Sandahl Sørensen подчертава, че е „решаващо за бъдещето на Европа фармацевтичната индустрия да остане на европейска земя“.
– Затова и се надявахме на споразумение, което да укрепи настоящите рамкови условия. Но напълно признаване усилията на датското правителство по време на преговорите, казва той в прессъобщение.
Той добавя, че със споразумението е успято да се „избегне съсипването на условията за европейската life science индустрия“.
Но той го вижда като стъпка в грешната посока в сравнение с условията, които САЩ предлагат на индустрията.
Life science обхваща основно фармацевтичната, биотехнологичната и медицинската област.
След като политическото споразумение е постигнато, пакетът за лекарствата сега трябва формално да бъде приет в началото на новата година.
След това държавите членки могат да започнат с прилагането.
 go to the original language article
go to the original language article